Την έναρξη της διεθνούς μελέτης Φάσης III START2 , ανακοίνωσε ο βιοφαρμακευτικός κλάδος της Merck Serono η οποία έχει σκοπό να αξιολογήσει την αποτελεσματικότητα και την ασφάλεια της ανοσοθεραπείας με το υπό έρευνα MUC1 ειδικό αντιγόνο L-BLP25 σε ασθενείς με μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο σταδίου ΙΙΙ μη μικροκυτταρικό καρκίνo του πνεύμονα (NSCLC).
Η δοκιμή START2 είναι μια πολυκεντρική, τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με placebo (εικονικό φάρμακο) μελέτη, σχεδιασμένη ώστε να αξιολογηθεί η αποτελεσματικότητα, η ασφάλεια και η ανεκτικότητα του L-BLP25 σε ασθενείς που υποφέρουν από μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο (Σταδίου ΙΙΙΑ ή ΙΙΙΒ) μη μικροκυτταρικό καρκίνο του πνεύμονα (NSCLC), οι οποίοι ανταποκρίθηκαν ή έδειξαν σταθερότητα στην ασθένειά τους μετά από τουλάχιστον δύο κύκλους ταυτόχρονης χημειο-ακτινοθεραπείας (CRT) με βάση την πλατίνα.
Η ταυτόχρονη χημειο-ακτινοθεραπεία – ένας συνδυασμός χημειοθεραπείας και ακτινοθεραπείας που παρέχονται ταυτόχρονα – είναι η τρέχουσα θεραπεία για τους περισσότερους από αυτούς τους ασθενείς. Η μελέτη αναμένεται να συμπεριλάβει περίπου 1.000 ασθενείς. Ο κύριος στόχος της μελέτης είναι η συνολική επιβίωση. Δευτερεύοντες στόχοι είναι ο χρόνος εξέλιξης των συμπτωμάτων, η επιβίωση χωρίς εξέλιξη της νόσου και ο χρόνος μέχρι την εξέλιξή της. Η Merck έλαβε Επιστημονική Γνωμοδότηση για το πρόγραμμα από τον Ευρωπαϊκό Οργανισμό Φαρμάκων (EMA) και κατέληξε σε συμφωνία με την Υπηρεσία Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ σχετικά με ένα Ειδικό Πρωτόκολλο Αξιολόγησης (SPA) για τη δοκιμή.
«Δυστυχώς, η θεραπεία του μη μικροκυτταρικού καρκίνου του πνεύμονα (NSCLC) σταδίου ΙΙΙ δεν βελτιώθηκε τα τελευταία χρόνια· νέες θεραπευτικές στρατηγικές είναι απαραίτητες επειγόντως», δήλωσε ο Καθηγητής Suresh Ramalingam, του Winship Cancer Institute, Emory University, Atlanta, ΗΠΑ, συντονιστής των κλινικών ερευνητών της μελέτης START2 και μέλος της αντίστοιχης οργανωτικής επιτροπής. «Η τροποποίηση του ανοσοποιητικού συστήματος ώστε να θεραπεύει τον καρκίνο μπήκε σε μια εξαιρετικά ενδιαφέρουσα νέα φάση τα τελευταία δύο με τρία χρόνια. Ελπίζουμε ότι η μελέτη START2 θα καθιερώσει το L-BLP25 ως μία νέα θεραπευτική επιλογή για ασθενείς με μη μικροκυτταρικό καρκίνο του πνεύμονα».
Η βάση της νέας Φάσης III μελέτης είναι το αποτέλεσμα της αρχικής μελέτης START.1 Με τη START δεν επετεύχθη το πρωτεύον καταληκτικό σημείο της συνολικής επιβίωσης με το L-BLP25 σε σύγκριση με το placebo στο σύνολο του πληθυσμού των ασθενών (n=1,239). Η μέση συνολική επιβίωση ήταν 25,6 μήνες για τους ασθενείς της ομάδας που λάμβανε L-BLP25 σε σύγκριση με τους 22,3 μήνες της ομάδας στην οποία χορηγούνταν placebo (προσαρμοσμένος σχετικός κίνδυνος [HR]: 0,88· 95% διάστημα εμπιστοσύνης [CI]: 0,75–1,03· p=0,123).
Ωστόσο, τα δεδομένα από μια διερευνητική ανάλυση μιας προκαθορισμένης υποομάδας της δοκιμής START, οι οποίοι λάμβαναν L-BLP25 μετά από ταυτόχρονη χημειο-ακτινοθεραπεία (CRT), έδειξαν ότι οι ασθενείς αυτής της υποομάδας πέτυχαν μια μέση συνολική επιβίωση 30,8 μηνών έναντι των 20,6 μηνών των ασθενών στους οποίους χορηγούνταν placebo (n=806, HR: 0,78; 95% CI 0,64–0,95; p=0,016).
Ο Δρ. John Orloff, Παγκόσμιος επικεφαλής του τμήματος Κλινικής Ανάπτυξης της Merck Serono, σχολίασε: «Σαφώς υπάρχει μεγάλη πραγματική ανάγκη επιπλέον θεραπευτικών επιλογών για ανθρώπους που αντιμετωπίζουν το μη μικροκυτταρικό καρκίνο του πνεύμονα. Τα αποτελέσματα της αρχικής μελέτης START έδωσαν επιστημονικές και κλινικές ενδείξεις με πληροφορίες για το σχεδιασμό αυτού του νέου προγράμματος Φάσης ΙΙΙ. Είμαστε ικανοποιημένοι που η START2 είναι τώρα σε εξέλιξη, και είμαστε πεπεισμένοι ότι αυτή η μελέτη θα καλύψει τα κενά στην κατανόηση του πιθανού ρόλου που το L-BLP25 θα μπορούσε να παίξει στη διαχείριση των ασθενών που ζουν με μη χειρουργήσιμο, μη μικροκυτταρικό καρκίνο του πνεύμονα σταδίου ΙΙΙ».
Το L-BLP25 είναι ένα υπό έρευνα MUC1 ειδικό αντιγόνο ανοσοθεραπείας καρκίνου που έχει σκοπό να διεγείρει το ανοσοποιητικό σύστημα του σώματος, ώστε να αναγνωρίζει και να στοχεύει τα καρκινικά κύτταρα που εκφράζουν τη γλυκοπρωτεΐνη επιφάνειας του κυττάρου MUC12,3. Η MUC1 εμφανίζεται σε πολλούς καρκίνους, συμπεριλαμβανομένου και του μη μικροκυτταρικού καρκίνου του πνεύμονα, και έχει πολλαπλούς ρόλους στην ανάπτυξη των όγκων και στην επιβίωση.2,4
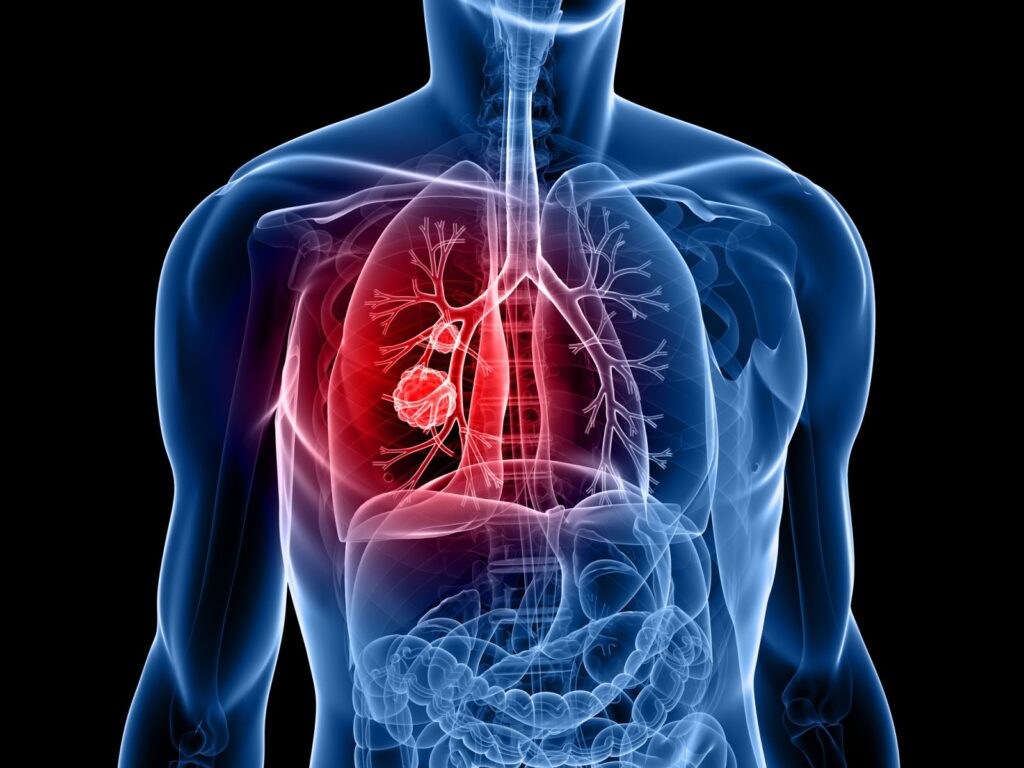
Σε παγκόσμιο επίπεδο, ο καρκίνος του πνεύμονα είναι η πιο κοινή αιτία θανάτου από καρκίνο στους άνδρες και η τρίτη πιο κοινή αιτία στις γυναίκες, και είναι υπεύθυνος για σχεδόν διπλάσιους θανάτους από εκείνους που οφείλονται συνολικά στους καρκίνους του μαστού και του προστάτη.5 Ο μη μικροκυτταρικός καρκίνος του πνεύμονα (NSCLC) είναι ο πιο συνηθισμένος τύπος καρκίνου του πνεύμονα, σε ποσοστό 80–85% όλων των τύπων καρκίνων του πνεύμονα, και ο τοπικά αναπτυγμένος ή ο Σταδίου ΙΙΙ υπολογίζεται σε ποσοστό περίπου 30% των ασθενών με αυτόν τον τύπο καρκίνου.6,7 Δυστυχώς, κατά τη διάγνωση, οι περισσότεροι ασθενείς έχουν προχωρημένη ή μεταστατική ασθένεια με πολύ κακή πρόγνωση.8
Σχετικά με το L-BLP25
Το L-BLP25 είναι ένα υπό έρευνα MUC1 ειδικό αντιγόνο ανοσοθεραπείας καρκίνου που έχει σκοπό να διεγείρει το ανοσοποιητικό σύστημα ώστε να αναγνωρίζει και να στοχεύει στα καρκινικά κύτταρα που εκφράζουν τη γλυκοπρωτεΐνη επιφάνειας του κυττάρου MUC1. Η MUC1 εμφανίζεται σε πολλούς καρκίνους, συμπεριλαμβανομένου και του μη μικροκυτταρικού καρκίνου του πνεύμονα, και έχει πολλαπλούς ρόλους στην ανάπτυξη των όγκων και στην επιβίωση. Το L-BLP25 ερευνάται τώρα στις δοκιμές Φάσης ΙΙΙ START2 και INSPIRE για τη χορήγησή του σε μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο μη μικροκυτταρικό καρκίνο του πνεύμονα (NSCLC) Σταδίου ΙΙΙ.
Η Merck απέκτησε τα αποκλειστικά παγκόσμια δικαιώματα για την ανάπτυξη και τη διάθεση στην αγορά του L-BLP25 από την Oncothyreon Inc., Seattle, Washington, ΗΠΑ, το 2007, με μια συμφωνία που αντικατέστησε προηγούμενες συμφωνίες συνεργασίας και προμήθειας που καταρτίσθηκαν αρχικά το 2001. Στην Ιαπωνία, η Merck προχώρησε σε συμφωνία για την από κοινού ανάπτυξη και κοινό μάρκετινγκ του L-BLP25 με την Ono Pharmaceutical Co., Ltd., Osaka, Ιαπωνία.
Η START2 είναι μια πολυκεντρική, 1:1 τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με placebo κλινική μελέτη Φάσης ΙΙΙ, που έχει σκοπό να αξιολογήσει την αποτελεσματικότητα, την ασφάλεια και την ανεκτικότητα του L-BLP25 σε ασθενείς που υποφέρουν από μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο (Σταδίου ΙΙΙΑ ή ΙΙΙΒ) μη μικροκυτταρικό καρκίνο του πνεύμονα (NSCLC), οι οποίοι ανταποκρίθηκαν ή έδειξαν σταθερότητα στην ασθένειά τους μετά από τουλάχιστον δύο κύκλους ταυτόχρονης χημειο-ακτινοθεραπείας (CRT) με βάση την πλατίνα. Ο κύριος στόχος της μελέτης είναι η συνολική επιβίωση.
Η αρχική Φάση ΙΙΙ της δοκιμής START είναι μια πολυκεντρική, τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με placebo κλινική δοκιμή, που έχει σκοπό να αξιολογήσει την αποτελεσματικότητα, την ασφάλεια και την ανεκτικότητα του L-BLP25 σε ασθενείς που υποφέρουν από μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο (Σταδίου ΙΙΙΑ ή ΙΙΙΒ) μη μικροκυτταρικό καρκίνο του πνεύμονα (NSCLC), οι οποίοι ανταποκρίθηκαν ή έδειξαν σταθερότητα στην ασθένειά τους μετά από τουλάχιστον δύο κύκλους χημειο-ακτινοθεραπείας (CRT) με βάση την πλατίνα (ταυτόχρονης ή διαδοχικής). Στη δοκιμή συμμετέχουν 1.239 ασθενείς από 33 χώρες. Ο κύριος στόχος της συνολικής επιβίωσης δεν επετεύχθη στη μελέτη START.
Η INSPIRE (L-BLP25 liposome vaccine trial In Asian NSCLC Patients: Stimulating Immune REsponse) είναι μια πολυκεντρική, τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με placebo κλινική μελέτη Φάσης ΙΙΙ, που έχει σκοπό να αξιολογήσει την αποτελεσματικότητα, την ασφάλεια και την ανεκτικότητα του L-BLP25 σε ασθενείς που υποφέρουν από μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο Σταδίου ΙΙΙΑ ή ΙΙΙΒ μη μικροκυτταρικό καρκίνο του πνεύμονα (NSCLC), οι οποίοι ανταποκρίθηκαν ή έδειξαν σταθερότητα στην ασθένειά τους μετά από τουλάχιστον δύο κύκλους ταυτόχρονης χημειο-ακτινοθεραπείας (CRT) με βάση την πλατίνα. Στην INSPIRE συμμετέχουν περίπου 500 ασθενείς με μη χειρουργικά εξαιρέσιμο, τοπικά αναπτυγμένο μη μικροκυτταρικό καρκίνο του πνεύμονα από την Κίνα, το Χονγκ Κονγκ, την Κορέα, τη Σιγκαπούρη και την Ταϊβάν.
Το L-BLP25 βρίσκεται τώρα υπό κλινική έρευνα και δεν έχει πάρει έγκριση για χρήση στις ΗΠΑ, την Ευρώπη, τον Καναδά ή αλλού. Το L-BLP25 δεν έχει αποδειχθεί ότι είναι ασφαλές ή αποτελεσματικό και οποιεσδήποτε διαβεβαιώσεις για την ασφάλεια και την αποτελεσματικότητα μπορούν να δοθούν μόνο μετά από έλεγχο των δεδομένων από τις αρμόδιες αρχές και έγκριση των αναφερομένων ενδείξεων.
Διαβάστε όλες τις τελευταίες Ειδήσεις για την υγεία από την Ελλάδα και τον ΚόσμοΑκολουθήστε το healthweb.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις
Ακολουθήστε το healthweb.gr στο κανάλι μας στο YouTube