Κορωνοϊός Παρενέργειες: Μια εφάπαξ δόση του φαρμάκου για την ηπατίτιδα C όταν ληφθεί νωρίς, θα μπορούσε να βοηθήσει τους ασθενείς Covid-19 να ανακάμψουν γρηγορότερα, και να αποφύγουν επιπλοκές που παρατηρήθηκαν στα προχωρημένα στάδια της νόσου, δήλωσε η Cadila Healthcare Ltd της Ινδίας.
Η Cadila Healthcare Ltd της Ινδίας ζήτησε έγκριση από τους τοπικούς ρυθμιστικούς φορείς, για να χρησιμοποιήσουν ένα φάρμακο για την ηπατίτιδα C ως θεραπεία για τον Covid-19, μετά από πολλά υποσχόμενα προσωρινά αποτελέσματα από μια δοκιμή στα τελικά στάδια, δήλωσε η φαρμακοβιομηχανία τη Δευτέρα.
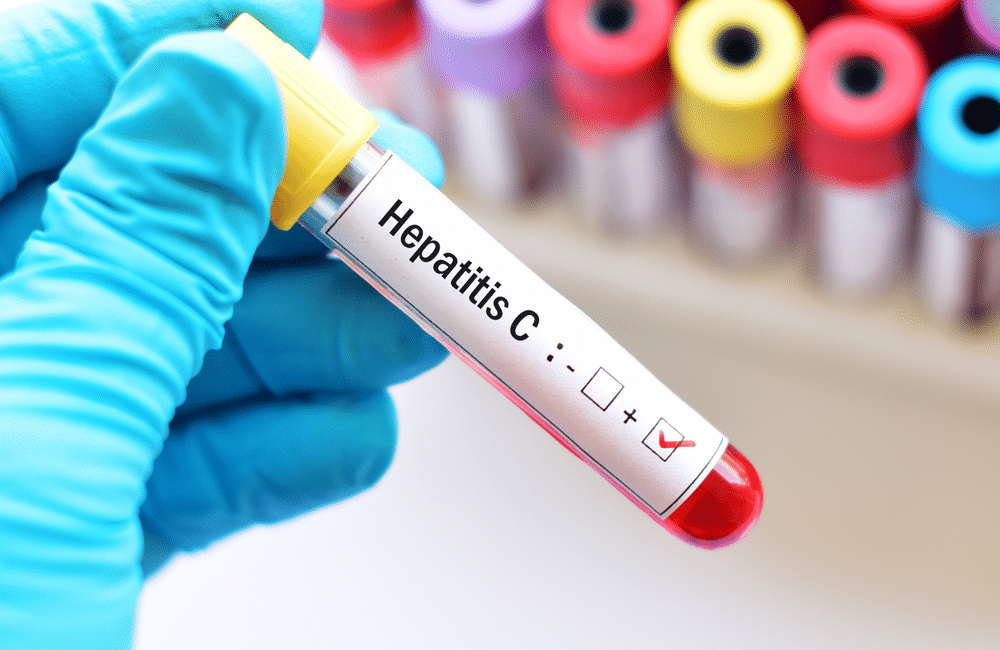
Μια εφάπαξ δόση του φαρμάκου για την ηπατίτιδα C, όταν λαμβάνεται νωρίς θα μπορούσε να βοηθήσει τους ασθενείς Covid-19 να ανακάμψουν γρηγορότερα, και να αποφύγουν επιπλοκές που παρατηρήθηκαν στα προχωρημένα στάδια της νόσου, σύμφωνα με δηλώσεις της φαρμακοβιομηχανίας. Περίπου το 91% των ασθενών που υποβλήθηκαν σε θεραπεία με το φάρμακο δοκιμάστηκαν αρνητικοί για τον Covid-19 σε τυπικές δοκιμές RT-PCR έως την 7η ημέρα, σε σύγκριση με σχεδόν το 79% στους οποίους δόθηκε το πρότυπο περίθαλψης, ανέφερε η εταιρεία επικαλούμενη δεδομένα κλινικών δοκιμών Φάσης-III.
Το φάρμακο, γνωστό ως Pegylated Interferon alpha-2b, που ονομάστηκε «PegiHep» από την Cadila, εγκρίθηκε αρχικά για ηπατική νόσο του ήπατος και κυκλοφόρησε στην Ινδία πριν από 10 χρόνια και επανατοποθετείται τώρα για τη θεραπεία του Covid-19. Τα νέα έρχονται καθώς οι καθημερινές μολύνσεις από κορονωϊό αυξάνονται δραματικά στην Ινδία, η οποίαωσημειωτέον έχει τον τρίτο υψηλότερο φορτίο στον κόσμο μετά τις Ηνωμένες Πολιτείες και τη Βραζιλία. Η Ινδία έχει μέχρι στιγμής αναφέρει περίπου 12,5 εκατομμύρια μολύνσεις και περισσότερους από 164.000 θανάτους.
Ακολουθεί βίντεο:
Διαβάστε όλες τις τελευταίες Ειδήσεις για την υγεία από την Ελλάδα και τον Κόσμο
Ακολουθήστε το healthweb.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις
Ακολουθήστε το healthweb.gr στο κανάλι μας στο YouTube